体外输注干细胞可修复损伤的血管,预防动脉粥样硬化!
2021-06-09
心血管疾病的诱因有很多种,今天我们来说说其中一种——动脉粥样硬化。动脉粥样硬化是动脉硬化性血管病中最常见、最重要的一种疾病,也是冠心病、脑卒中、外周动脉疾病(PAD)和肾病病理基础,在中老年群体中更为普遍。
动脉粥样硬化(AS)是一种典型的慢性炎症性血管病变,主要影响动脉内膜,由于脂质成分和炎性物质沉积在动脉血管内壁,形成外观像小米粥样的斑块,导致动脉变窄变硬、弹性降低、阻碍血流,继而造成器官缺血损伤。
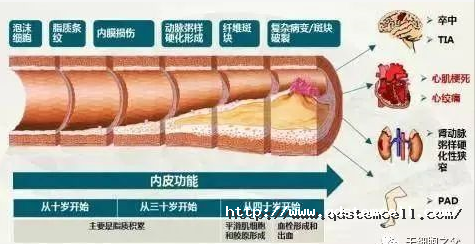
动脉粥样硬化的发展是一个缓慢持续进行的过程,初期动脉粥样硬化常无临床症状,容易被忽视,一旦发展到血栓严重阻塞动脉腔时,则该动脉所供应的组织或器官将缺血或坏死。会诱发严重疾病,包括冠心病(心绞痛、心肌梗死)、脑卒中以及外周血管疾病。动脉粥样硬化病因复杂,基于细胞层面的微观分析,动脉内皮细胞功能发生障碍是动脉粥样硬化病变的第一步,血管壁内皮损伤如果不能及时修复,就会引发炎症以及粥样斑块的产生,而炎症反应在动脉粥样硬化的发生及其并发症形成过程中起着重要作用。
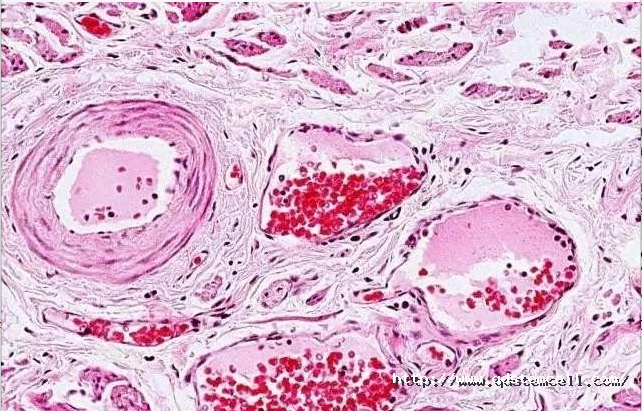
此外,血管平滑肌细胞的异常改变在动脉粥样硬化的发生发展中也扮演着重要角色,大量研究显示动脉粥样硬化中增殖的平滑肌细胞是血管中膜平滑肌细胞受到各种病理刺激后发生表型改变、迁移进入内膜后聚集、增殖而来。除去年龄和家族病史外,具有胆固醇水平异常、甘油三酯偏高、高血压、吸烟、胰岛素抵抗、糖尿病、超重或肥胖等高危因素人群更容易患动脉粥样硬化。早期的可以用他汀类药物治疗,症状严重时也可以经外科手术(俗称“搭桥”)或介入(俗称“放支架”)治疗。
由于临床使用的抗AS药物存在肝肾损伤、横纹肌溶解等副作用,如何攻克它成为临床医学的研究重点。生物医学领域的科学家一直在探讨新的防治方式,而干细胞疗法的出现成功解决这一难题。科学家通过临床治疗发现,干细胞具有调节血脂水平、抑制炎症、修复受损组织和支持造血的功能,对血管损伤、血管炎症具有有益的修复调节作用。越来越多的研究表明干细胞具有修复损伤组织的潜能,干细胞技术的发展为损伤血管修复提供了新方向。近年来有研究发现,间充质干细胞 ( MSCs)可以分化为内皮细胞,加速受损内皮修复,抑制动脉狭窄的形成。
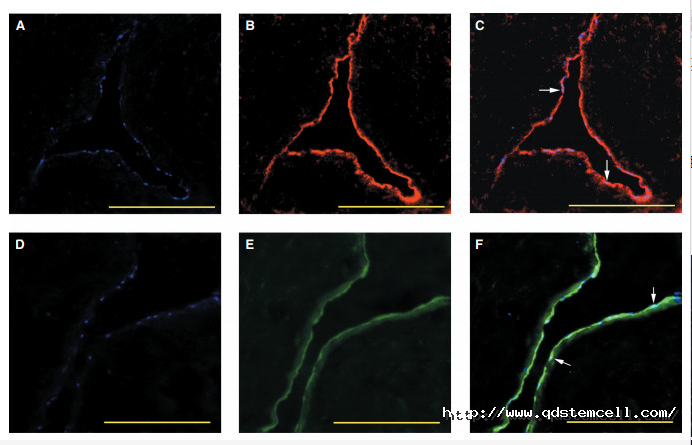
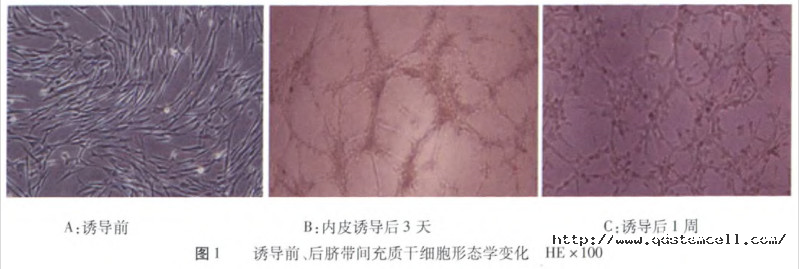
【间充质干细胞治疗后,切片显示移植细胞参与修复血管,向内皮细胞分化(图b)】体外输注的间充质干细胞能够向受损部位募集,并进一步分化为内皮细胞,修复损伤血管。另一项研究也证实了干细胞对于血管新生产生的作用。

研究发现脐带组织中提取出的干细胞,能够在缺血微环境条件下分化成内皮细胞,参与血管新生,促进缺血局部的血流恢复。
在《中华老年心脑血管病杂志》发布的最新研究综述,阐述了干细胞移植防治动脉粥样硬化的研究进展。论文第一作者总结了干细胞移植降低动脉粥样硬化风险的4大机制:专家通过对高胆固醇血症模型小鼠进行干细胞移植移植,8周后数据表明,干细胞移植后的小鼠血清胆固醇水平下降了33%。通过实验证明,干细胞可增强内皮细胞分化,提高内皮细胞活力,加速受损动脉内膜的修复过程,减少或消除斑块的堆积。干细胞移植能清除炎症细胞进而减缓AS进程,主要表现为减少浸润的炎性巨噬细胞迁移、抑制其活化、改变巨噬细胞的可塑性、打破 M1 / M2 的平衡、调节T/B细胞的免疫平衡。在AS的修复过程中提供营养物质,干细胞移植支持造血功能,加速体内的营养物质交换,提高血管修复效率,促进新血管的生成。据ClinicalTrials.gov数据显示 ,目前已启动超10项干细胞移植的临床试验项目,应用于动脉粥样硬化的研究工作。近10年临床试验证实:干细胞移植可缓解动脉粥样硬化的发展,减轻炎症的介质的产生,大大降低了心脑血管疾病的发生风险。随着对干细胞临床治疗的进一步研究,相信未来将造福更多动脉粥样硬化患者。





